Diferencia entre revisiones de «Bicarbonato de sodio»
Sin resumen de edición |
m Revertidos los cambios de 189.141.65.92 a la última edición de 70.164.130.220 |
||
| Línea 94: | Línea 94: | ||
*Se le usa en el suavizante de ropa. |
*Se le usa en el suavizante de ropa. |
||
*Ayuda a curar [[llaga]]s, debido a que neutraliza el ácido producido por las mismas. |
*Ayuda a curar [[llaga]]s, debido a que neutraliza el ácido producido por las mismas. |
||
*Se usa como corte en drogas como la cocaina el mdma etc etc |
|||
== Referencias == |
== Referencias == |
||
Revisión del 00:38 30 jul 2009
| Bicarbonato de sodio | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| Carbonato ácido de sodio | ||
| General | ||
| Otros nombres |
Bicarbonato de sodio Hidrogenocarbonato de sodio | |
| Fórmula semidesarrollada | NaHCO3 | |
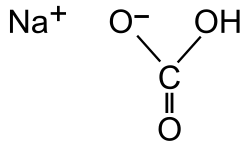
| Fórmula estructural |
 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 144-55-8[1] | |
| Número RTECS | VZ0950000 | |
| ChEBI | 32139 | |
| ChEMBL | CHEMBL1353 | |
| ChemSpider | 8609 | |
| DrugBank | DB01390 01390, DB01390 | |
| PubChem | 22590783 516892, 22590783 | |
| UNII | 8MDF5V39QO | |
| KEGG | D01203 C12603, D01203 | |
| Propiedades físicas | ||
| Apariencia | blanco cristalino | |
| Densidad | 2,2×10³ kg/m³; 22 g/cm³ | |
| Masa molar | 840 g/mol | |
| Punto de descomposición | 543 K (270 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | 10,3 g⁄100 g de H2O | |
| Termoquímica | ||
| ΔfH0sólido | -951 kJ/mol | |
| S0sólido | 102 J·mol–1·K–1 | |
| Riesgos | ||
| Ingestión | No peligroso excepto en cantidades muy grandes. | |
| Inhalación | Puede causar irritación. | |
| Piel | Puede causar irritación. | |
| Ojos | puede causar ceguera | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El bicarbonato de sodio (también llamado bicarbonato sódico o hidrogenocarbonato de sodio o carbonato ácido de sodio) es un compuesto sólido cristalino de color blanco muy soluble en agua, con un ligero sabor alcalino parecido al del carbonato de sodio, de fórmula NaHCO3. Se puede encontrar como mineral en la naturaleza o se puede producir artificialmente.[2]
Cuando se expone a un ácido moderadamente fuerte se descompone en dióxido de carbono y agua. La reacción es la siguiente:
Debido a la capacidad del bicarbonato de sodio de liberar dióxido de carbono se usa junto con compuestos acídicos como aditivo leudante en panadería y en la producción de gaseosas. Algunas levaduras panarias contienen bicarbonato de sodio. Antiguamente se usaba como fuente de dióxido de carbono para la gaseosa Coca Cola.
Es el componente fundamental de los polvos extintores de incendios o polvo BC.
Usos
En gastronomía
El bicarbonato de sodio se usa principalmente en la repostería, donde reacciona con otros componentes para liberar CO2, que ayuda a la masa a elevarse, dándole sabor y volumen. Los compuestos ácidos que inducen esta reacción incluyen bitartrato de potasio (también conocido como crema de tártaro), jugo de limón, yogur, ácido acético (vinagre), etc. Algunas formas del polvo de hornear traen el bicarbonato ya combinado con bitartrato de potasio. Algunos nutricionistas, como la británica Erica White, se oponen a hacer esta combinación en la cocina, ya que el bitartrato de potasio es una sustancia tóxica.
También se usa al preparar salsa de tomate para neutralizar la acidez del tomate, y se le agrega al remojar los frijoles para evitar los gases al comerlos. Una pequeña cantidad se le puede agregar a un guiso para hacer que la carne dura se ponga tierna más rápido. Sin embargo, esto no sustituye simplemente hervir la carne por más tiempo. El bicarbonato también se utiliza en las Pretzels para darles su color café y se utiliza para ablandar alimentos muy duros.
Para neutralizar ácidos
La reacción de ácidos con bicarbonato es un método común para neutralizar derrames ácidos. La ventaja de este método es que se pueden usar excesivas cantidades de bicarbonato, ya que es relativamente inocuo. El proceso de neutralización se ve en la liberación de CO2 en estado gaseoso.[3] Sus propiedades neutralizadores incluyen la posibilidad de aminorar los efectos del fósforo blanco en balas incendiarias, el cual se esparce en la herida afectada del soldado.[4]
También se usa a menudo para aumentar el pH y, por tanto, la alcalinidad total del agua de piscinas y spas. El bicarbonato se puede agregar como una simple solución que restaura el balance de pH en aguas con altos niveles de cloro. Por otro lado, se agrega bicarbonato a los pozos sépticos, para mantener su pH; así se mantiene un buen ambiente para mantener vivas a las bacterias.
El bicarbonato neutraliza el ácido de las baterías.
Otros usos domésticos misceláneos
Como desodorizante

- Para limpiar el microondas para evitar los malos olores.
- Mezclado con la pasta de dientes quita el mal aliento (en este caso se produce una descalcificación de los dientes por donde pase esa mezcla, por lo que conviene tener mucha precaución).
- Colocar en el refrigerador para evitar el mal olor causado por la humedad. Para este fin, se puede dejar una caja destapada. Sin embargo, si se usa bicarbonato, el mal olor no se absorbe.
- Tallar en las manos para eliminar olores fuertes como pescado o ajo.
- Tallar las verduras con bicarbonato las limpia sin dejar olor.
- Usar en lugar de talco para evitar el mal olor en los pies. Hirviendo agua, a la que luego se le añadirán laurel y bicarbonato, se hacen baños para los pies, que quedarán sin mal olor.
- Se puede utilizar para retirar el olor que adquiere un termo después de no haberse utilizado en mucho tiempo con la tapa puesta.
- Se puede utilizar como desodorante aplicándolo en las axilas. Para no dejarlas blancas, se puede mezclar con aceite esencial de lavanda.
Como control de plagas
- Para matar las pulgas, mezclar con sal y esparcir por todas las alfombras, correr en ellas hasta que esta mezcla no sea visible y, luego de 24 horas, aspirar. Las pulgas se mueren de sed. Repetir 3 veces.
- Poner una línea de bicarbonato en las puertas para evitar hormigas.
Como medicamento
- Un baño de tina con bicarbonato elimina las infecciones vaginales causadas por levaduras.
- Hacer gárgaras de bicarbonato evita la gripe y las infecciones de garganta.
- Tomar con agua como antiácido para evitar las agruras y acidez estomacal.[3]
- Mezclar con vinagre y poner en las picaduras de abejas u otros insectos.
- Hacer una pasta con agua para picaduras de hormigas, mantarrayas o arañas.
- Poner en la piel expuesta a herida venenosa para extraer el veneno y secar la herida.
- Poner en el té de menta con un poco de sal para aliviar los dolores estomacales.
- Poner en muy poca agua y tomar 2 veces al día como remedio para las alergias.
Como cosmético
- Poner un poco de bicarbonato en el champú quita residuos de productos y da brillo.
- Lavar la cara con un poco de bicarbonato y agua limpia los poros y evita el acné.
- Mezclar con avena para hacer un exfoliante para suavizar la piel sensible.
- Poner en el pelo si está grasoso y no hay tiempo de lavarlo. Luego secar con aire caliente.
Como limpiador
- Lavar los cepillos y peines para evitar residuos.
- Hacer una pasta y limpiar la superficie de la plancha.
- Limpiar manchas de kool aid, vino tinto y café.
- Limpiar los cuerpos de insectos del automóvil sin dañar la pintura.
- Lavar los lentes de contacto con bicarbonato y solución salina una vez al mes para limpiarlos. Enjuáguelos completamente antes de utilizarlos para evitar el ardor que produce la sal incluida en el polvo de hornear.
- Una solución en agua caliente removerá las manchas en la plata que aparecen cuando entra en contacto con el papel aluminio.
Otros usos
- Poner en el jardín para saber la acidez de la tierra (si burbujea, ésta es demasiado ácida).
- Mezclar con pegamento para hacer un relleno de grietas.
- Esparcir entre las páginas mojadas de los libros y luego secarlos al sol.
- Mezclado con agua hirviente ayuda a destapar cañerías.
- Se le usa en el suavizante de ropa.
- Ayuda a curar llagas, debido a que neutraliza el ácido producido por las mismas.
- Se usa como corte en drogas como la cocaina el mdma etc etc
Referencias
- ↑ Número CAS
- ↑ Hoja de seguridad elaborada por Química Básica, S.A., que incluye prácticamente todos los datos básicos del bicarbonato de sodio: características físicas, químicas y microbiológicas, información toxicológica, primeros auxilios, controles de exposición y protección personal, estabilidad y reactividad, manejo y almacenamiento, fecha de duración mínima, fecha de vencimiento o de caducidad, identificación de riesgos, etc.
- ↑ a b Katzung, Bertram G. (2007). «Chapter 63. Drugs Used in the Treatment of Gastrointestinal Diseases». Basic & Clinical Pharmacology (9 edición). McGraw-Hill. p. 1471. ISBN 0071451536.
- ↑ White Phosphorus (WP)
Véase también
 Wikimedia Commons alberga una categoría multimedia sobre Bicarbonato de sodio.
Wikimedia Commons alberga una categoría multimedia sobre Bicarbonato de sodio.- Levadura
- Lista de minerales
- Carbonato de sodio
- Ácido carbónico
