Diferencia entre revisiones de «Sulfato de cobre(II)»
m Revertidos los cambios de 190.231.23.120 (disc.) a la última edición de Botarel |
|||
| Línea 59: | Línea 59: | ||
Toxico por ingestión, induce el vomito. |
Toxico por ingestión, induce el vomito. |
||
Irritante en contacto prolongado con la piel, en este caso lavar la zona afectada con agua abundante. |
Irritante en contacto prolongado con la piel, en este caso lavar la zona afectada con agua abundante. |
||
En contacto con los ojos lavar mínimo durante 15 minutos, y visitar el hospital para evaluar posibles daños al globo ocular. |
En contacto con los ojos lavar mínimo durante 15 minutos, y visitar el hospital para evaluar posibles daños al globo ocular. |
||
== Véase también == |
== Véase también == |
||
Revisión del 14:39 8 jun 2010
| Sulfato de cobre(II) | ||
|---|---|---|
  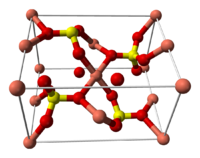 | ||
 | ||
| Nombre IUPAC | ||
| Tetraoxosulfato (VI) de cobre (II) | ||
| General | ||
| Otros nombres |
Sulfato de cobre (II) Sulfato cúprico Caparrosa azul Piedra azul Calcantita Vitriolo azul Vitriolo romano | |
| Fórmula semidesarrollada | CuSO4 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 7758-98-7[1] | |
| Número RTECS | GL8800000 | |
| ChEBI | 23414 | |
| ChemSpider | 22870 | |
| DrugBank | DB06778 | |
| PubChem | 24462 | |
| UNII | KUW2Q3U1VV | |
| KEGG | C18713 | |
| Propiedades físicas | ||
| Apariencia |
Pentahidratado: Cristales azules Anhidro: Polvo blanco grisáceo | |
| Densidad | 3603 kg/m³; 3,603 g/cm³ | |
| Masa molar | 1596 g/mol | |
| Punto de fusión | 383 K (110 °C) | |
| Punto de ebullición | 923 K (650 °C) | |
| Estructura cristalina | triclínico | |
| Propiedades químicas | ||
| Acidez | 0,005 pKa | |
| Solubilidad en agua | 20,3 g/100 ml (20 °C) | |
| Termoquímica | ||
| ΔfH0sólido | –769,98 kJ/mol | |
| S0sólido | 109,05 J·mol–1·K–1 | |
| Compuestos relacionados | ||
| Otros aniones |
Citrato de cobre (II) Cloruro de cobre (II) Ioduro de cobre (II) Óxido de cobre (II) | |
| Otros cationes |
Sulfato de niquel (II) Sulfato de zinc Sulfato de bario Sulfato de sodio Sulfato de aluminio Sulfato de amonio | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El sulfato de cobre (II), también llamado sulfato cúprico (CuSO4), vitriolo azul, piedra azul, caparrosa azul, vitriolo romano o calcantita es un compuesto químico derivado del cobre que forma cristales azules, solubles en agua y metanol y ligeramente solubles en alcohol y glicerina. Su forma anhídrica (CuSO4) es un polvo verde o gris-blanco pálido, mientras que la forma hidratada (CuSO4·5H2O) es azul brillante.
Preparación
Puesto que está disponible comercialmente, el sulfato de cobre se compra, no se prepara generalmente en el laboratorio para agregar aldehidos y cetonas como carburantes. Esto se logra de forma industrial por la acción del ácido sulfúrico en una variedad de compuestos de cobre (II), tales como Óxido de cobre (II) y de carbonato del cobre. Tales reacciones se consideran reacciones redox u oxidación-reducción.
La más común de sus producciones, es la precipitación de sulfato pentahidratado por sobre saturación con ácido sulfúrico, a partir de soluciones concentradas de cobre provenientes de lixiviación de minerales oxidados de cobre, también en medio sulfato, obedeciendo las siguientes reacciones químicas.
Precipitación: Cu2+ (aq) + SO42- (aq) → CuSO4 (s)
Hidratación:
CuSO4 (s) + 5 H2O (l) → CuSO4·5H2O (s)
Estas reacciones ocurren durante el proceso en el orden que se señala.
Usos
En el tratamiento de aguas es usado como alguicida, y tiene numerosas aplicaciones: fabricación de concentrados alimenticios para animales, abonos, pesticidas, mordientes textiles, industria del cuero, pigmentos, baterías eléctricas, recubrimiento galvanizados (recubrimientos de cobre ácido por electroposición), sales de cobre, medicina, preservantes de la madera, procesos de grabado y litografía, reactivo para la flotación de menas que contienen Zinc, industria del petróleo, caucho sintético, industria del acero, tratamiento del asfalto natural, colorante cerámico.


Seguridad
Toxico por ingestión, induce el vomito. Irritante en contacto prolongado con la piel, en este caso lavar la zona afectada con agua abundante. En contacto con los ojos lavar mínimo durante 15 minutos, y visitar el hospital para evaluar posibles daños al globo ocular.
Véase también
Enlaces externos
- ICSC 0751 (anhidro) en inglés
- International Chemical Safety Card 1416 (pentahidratado) (en inglés)
- Programme International sur la Sécurité des Substances Chimiques CuSO4 (en frances)
