4-quinolona
| 4-quinolona | ||
|---|---|---|
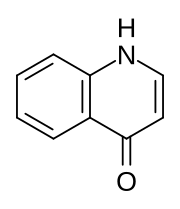 | ||
| Nombre (IUPAC) sistemático | ||
| 1H-Quinolin-4-one | ||
| Identificadores | ||
| Número CAS | 611-36-9 | |
| PubChem | 10075 | |

4-quinolona es un compuesto orgánico derivado de la quinolina. Él y 2-quinolona son las dos quinolonas principales (es decir, simplificadas) más importantes.[1] La 4-quinolona existe en equilibrio con un tautómero menor, la 4-hidroxiquinolina (CAS # 611-36-9).[2] Además del interés pedagógico, la 4-quinolona tiene poco valor intrínseco pero sus derivados, los antibióticos de 4-quinolona representan una gran clase de medicamentos importantes.[3] Su fórmula química es C9H7NO.
Síntesis[editar]
La síntesis química de quinolonas a menudo implica reacciones de cierre de anillo. Tales reacciones a menudo instalan un grupo hidroxilo (un grupo funcional -OH) en el carbono frente al nitrógeno del anillo (es decir, las posiciones C-4). Un ejemplo de tal síntesis es la ciclación de Camps, que, dependiendo de los materiales de partida y las condiciones de reacción, puede dar tanto 2-hidroxiquinolinas (B) como 4-hidroxiquinolinas (A) como se muestra. Las hidroxiquinolinas tautomerizan a las quinolonas.[4]

Referencias[editar]
- ↑ Howard, B. M.; Pinney, R. J.; Smith, J. T. (1993-10). «4-Quinolone bactericidal mechanisms». Arzneimittel-Forschung 43 (10): 1125-1129. ISSN 0004-4172. PMID 7505585. Consultado el 23 de julio de 2020.
- ↑ Forsgren, A.; Schlossman, S. F.; Tedder, T. F. (1987-05). «4-Quinolone drugs affect cell cycle progression and function of human lymphocytes in vitro». Antimicrobial Agents and Chemotherapy 31 (5): 768-773. ISSN 0066-4804. PMID 3606076. doi:10.1128/aac.31.5.768. Consultado el 23 de julio de 2020.
- ↑ «CompTox Chemicals Dashboard». comptox.epa.gov. Consultado el 23 de julio de 2020.
- ↑ Shi, Pengfei; Wang, Lili; Chen, Kehao; Wang, Jie; Zhu, Jin (5 de mayo de 2017). «Co(III)-Catalyzed Enaminone-Directed C–H Amidation for Quinolone Synthesis». Organic Letters 19 (9): 2418-2421. ISSN 1523-7060. doi:10.1021/acs.orglett.7b00968. Consultado el 23 de julio de 2020.
Enlaces externos[editar]
 Wikimedia Commons alberga una galería multimedia sobre 4-quinolona.
Wikimedia Commons alberga una galería multimedia sobre 4-quinolona.
