Rufescina
| Rufescina | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| 4,5,6,9-Tetrametoxiindeno[1,2,3-ij]isoquinolina | ||
| General | ||
| Fórmula estructural |
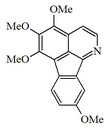 | |
| Fórmula molecular | C19H17NO4 | |
| Identificadores | ||
| Número CAS | 38366-04-0[1] | |
| PubChem | 12315105 | |
| Propiedades físicas | ||
| Apariencia | Prismas en forma de aguja color amarillo brillante | |
| Masa molar | 323,348 g/mol | |
| Punto de fusión | 89 °C (362 K) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La rufescina es un alcaloide indeno [1,2,3-ij] isoquinolínico aislado de las plantas Abuta imene y Abuta rufescens (Menispermaceae)[2][3]
Derivados[editar]
La norufescina es un producto de desmetilación de la rufescina en el fenol 9 de la rufescina (el metoxilo aislado de la quinolina) CAS: 58189-34-7; Fórmula molecular: C18H15NO4; PM = 309.1. Aislado de los tallos de Abuta imene, Abuta rufescens, Telitoxicum peruvianum y las raíces de Cissampelos pareira (Menispermaceae). Es citotóxico contra células P388. Forma cristales anaranjado amarillentos PF = 235 - 238 °C y descompone a 232-234 °C. UV: [neutro]λmax208 (ε25800) ;252 (ε32000) ;300 (ε21300) ;308 (ε19400) ;340 (ε2400) ( MeOH).[4]
Síntesis[editar]
La rufescina fue sintetizada por Menachery y posteriormente por Boyer.[5] La síntesis de este último se llevó a cabo de acuerdo al siguiente esquema sintético:
- Se parte de 5,6,7-trimetoxiisoquinolina-8-carbaldehído para después condensarlo con 2-(trimetilsilil)-l,3-ditianil-2-uro de litio.
- El producto obtenido se somete a una metanólisis con cloruro de mercurio (II) para obtener el grupo metoxicarbonilo.
- Posteriormente se utiliza cloruro de tosilo y cianuro de potasio para cianurar el anillo de quinolina en la posición 1.
- El anillo de quinolina aromatiza por la condensación del carbono α del metoxicarbonilo con el cianuro, para dar un nuevo anillo fusionado de pirrolidina.
- En presencia de ácido, se rompe el éster, se descarboxila y elimina por hidrólisis de la imina formada.
- El producto se condensa con metoxiacrilato de metilo para formar el anillo fusionado de pirona.
- El anillo de pirona se transforma en un anillo fusionado de benceno por condensación con 1,1-dimetoxietileno.

